18e survey des organismes notifiés : quel bilan pour la disponibilité des dispositifs médicaux dans l'UE ?
- il y a 16 heures
- 1 min de lecture
Un système qui progresse, mais des délais encore importants
La 18e enquête européenne auprès des organismes notifiés, arrêtée au 31 octobre 2025, apporte un éclairage sur l'état de la certification MDR dans l'Union européenne. Si la capacité du système progresse, les délais restent loin d'être optimaux.

Les chiffres clés au 31 octobre 2025
Les données publiées font apparaître un écart significatif entre les demandes déposées et les certificats effectivement émis :
33 175 Demandes MDR déposées
17 549 Certificats MDR émis
L'écart reste important, même en tenant compte des dossiers retirés, refusés ou modifiés. Une part significative des portefeuilles fabricants demeure donc en attente, avec un risque de retard d'accès au marché.
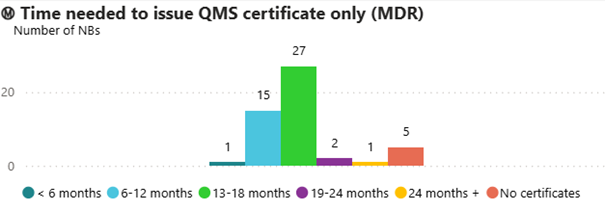
Des délais particulièrement élevés pour certaines évaluations
Les évaluations QMS seul et QMS + produit sont les plus concernées par ces délais. Cette situation a des implications directes pour les fabricants dont les échéances réglementaires approchent.
Ce que cela signifie pour les fabricants
Ces données confirment trois points d'attention majeurs pour tout fabricant opérant sous le règlement MDR :
Les renouvellements critiques et extensions de gamme restent particulièrement sensibles aux délais de certification.
Les stratégies d'accès au marché doivent anticiper ces délais dès la phase de planification.
Les portefeuilles produits nécessitent un pilotage réglementaire proactif pour éviter toute rupture de disponibilité.
Consultez les autres articles de veille réglementaire.


